Pembahasan Soal Kimia SBMPTN 2018 Nomor 43 PDF DOC Persiapan SBMPTN 2019 | Asam-basa Konjugasi dan Asam-basa Lewis

Pembahasan Soal Kimia SBMPTN 2018 Nomor 43 PDF DOC Persiapan SBMPTN 2019 | Asam-basa Konjugasi dan Asam-basa Lewis – Pelaksanaan SBMPTN 2019 sebentar lagi akan digelar. Berbagai Persiapan SBMPTN 2019 dari murid-murid yang mengharapkan kampus negeri mulai dilakukan. Salah satunya adalah mencari soal dan Pembahasan Soal Kimia SBMPTN 2018. Dalam beberapa tulisan ke depan kita fokus bahas soal SBMPTN Kimia 2018. Alhamdulillah pak urip.info sudah rilis pembahasan soal SBMPTN 2018 jadi bisa menambah wawasan kita dalam Persiapan SBMPTN 2019.
Pembahasan Soal Kimia SBMPTN 2018 Nomor 43 PDF DOC Persiapan SBMPTN 2019 | Asam-basa Konjugasi dan Asam-basa Lewis
Dalam tulisan kali ini, khusus untuk Soal SBMPTN Kimia Nomor 43 dengan pokok bahasan Asam-basa Konjugasi dan Asam-basa Lewis.
Perlu diingat bahawa pengertian Asam Brownsted-Lowry adalah zat yang mampu mendonorkan proton (H+) kepada zat atau spesi lain, sedangkan pengertian basa Bronsted-Lowry adalah zat yang menerima proton dari zat lain.
Pasangan asam basa konjugasi memiliki ciri kemiripan rumus kimia dengan selisih jumlah H sebanyak satu atom H. Asam-basa konjugasi ini berdasarkan konsep asam-basa Bronsted-Lowry.
Pengertian Basa Lewis adalah zat yang mendonorkan pasangan elektron kepada zat lain. Pasangan elektron yang didonorkan itu digunakan bersama dalam membentuk ikatan kovalen koordinasi.
Pengertian Asam Lewis zat yang dapat menerima pasangan elektron dari zat lain.
Syarat sebagai basa Lewis harus mempunyai pasangan elektron bebas dan syarat sebagai asam Lewis harus mempunyai orbital kosong pada atom pusatnya.
Catatan: untuk soal nomor 31, 39, dan 41 tidak dibahas khusus oleh pak URIP.INFO, silakan dibaca pada pembahasan soal disini.
Soal Kimia SBMPTN 2018 Nomor 34 Kode: 402, 429, 444, 452 | Persiapan SBMPTN 2019
Berdasarkan reaksi berikut:
CH3OH(aq) + C2H3O2–(aq) ⇌ HC2H3O2(aq) + CH3O–(aq)
HC2H3O2(aq) + CO32–(aq) ⇌ HCO3– + C2H3O2–(aq)
C6H5NH3+(aq) + OH– (aq) ⇌ C6H5NH2(aq) + H2O(l)
Yang bukan pasangan asam-basa konjugasi yaitu ….
(A) CH3OH dan CH3O–
(B) HC2H3O2dan HCO3–
(C) C6H5NH2 dan C6H5NH3+
(D) C2H3O2– dan HC2H3O2
(E) HCO3– dan CO32–
Pembahasan Soal Kimia SBMPTN 2018 Nomor 34 Kode: 402, 429, 444, 452
Ciri dari pasangan asam basa konjugasi yaitu memiliki kemiripan rumus kimia dengan selisih jumlah H sebanyak satu atom H.
Yang bukan pasangan asam-basa konjugasi yaitu HC2H3O2 dan HCO3–
Persiapan SBMPTN 2019 | Kunci Jawaban Soal Kimia SBMPTN 2018 Nomor 34 B
Soal Kimia SBMPTN 2018 Nomor 34 Kode: 403, 423, 453, 459, 461 | Persiapan SBMPTN 2019
Ion Al3+ dalam air terhidrasi membentuk ion kompleks [Al(H2O)6]3+(aq). Ion kompleks tersebut dapat menetralkan ion hidroksida menurut reaksi berikut.
[Al(H2O)6]3+ + OH– ⇌ [Al(H2O)5OH]2+ + H2O
[Al(H2O)5OH]2+ + OH– ⇌ [Al(H2O)4(OH)2]+ + H2O
[Al(H2O)4(OH)2]+ + OH– ⇌ Al(H2O)3(OH)3 + H2O
Manakah pernyataan yang benar dari fakta di atas?
(A) [Al(H2O)6]3+ bertindak sebagai basa Lewis
(B) [Al(H2O)4(OH)2]+ merupakan basa konjugasi dari Al(H2O)3(OH)3
(C) Pada semua reaksi tersebut H2O bersifat basa
(D) [Al(H2O)4(OH)2]+ bersifat amfiprotik
(E) Al(H2O)3(OH)3 merupakan asam konjugasi dari [Al(H2O)6]3+
Pembahasan Soal Kimia SBMPTN 2018 Nomor 34 Kode: 403, 423, 453, 459, 461
Pengertian Basa Lewis yaitu zat yang mendonorkan pasangan elektron kepada zat lain untuk digunakan bersama dalam membentuk ikatan kovalen koordinasi.
Pengertian Asam Lewis zat yang dapat menerima pasangan elektron dari zat lain.
Syarat sebagai basa Lewis harus mempunyai pasangan elektron bebas dan syarat sebagai asam Lewis harus mempunyai orbital kosong pada atom pusatnya.
Pada proses hidrasi air mendonorkan PEB kepada ion Al3+ sebanyak 6 molekul, jadi air di sini berperan sebagai basa Lewis, dan ion Al3+sebagai asam Lewis.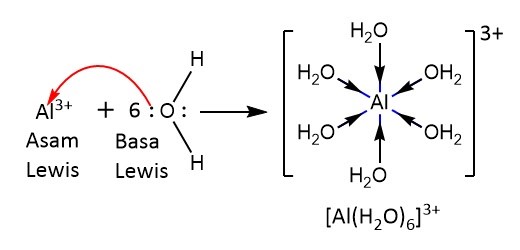 Dari pilihan yang tersedia dan fakta maka air dalam semua reaksi bersifat sebagai basa.
Dari pilihan yang tersedia dan fakta maka air dalam semua reaksi bersifat sebagai basa.
Persiapan SBMPTN 2019 | Kunci Jawaban Soal Kimia SBMPTN 2018 Nomor 34 C.
Soal Kimia SBMPTN 2018 Nomor 34 Kode: 412 | Persiapan SBMPTN 2019
Dalam reaksi berikut:
HNO2 + H2O ⇌ NO2– + H3O+
HPO42– + SO32– ⇌ PO43– + HSO3–
HNO2 + PO43– ⇌ NO2– + HPO42–
yang merupakan pasangan asam-basa konjugasi yaitu ….
(A) HPO42– dan PO43–
(B) HNO2 dan H3O+
(C) NO2– dan PO43–
(D) HNO2 dan HPO42–
(E) H2O dan HSO3–
Pembahasan Soal Kimia SBMPTN 2018 Nomor 34 Kode: 412
Ciri dari pasangan asam basa konjugasi yaitu kemiripan rumus kimia dengan selisih jumlah H sebanyak satu atom H.
Persiapan SBMPTN 2019 | Kunci Jawaban Soal Kimia SBMPTN 2018 Nomor 34 A.
Soal Kimia SBMPTN 2018 Nomor 34 Kode: 418, 460, 463 | Persiapan SBMPTN 2019
Dalam reaksi berikut:
HSO4–(aq) + H2O(l) ⇌ H3O+(aq) + SO42–(aq)
CH3COOH(aq) + HI(aq) ⇌ CH3COOH2+(aq) + I–(aq)
H2O (l) + S2–(aq) ⇌ OH–(aq) + HS–(aq)
yang bukan merupakan pasangan asam-basa konjugasi yaitu ….
(A) HSO4– dan SO42–
(B) H2O dan H3O+
(C) CH3COOH dan CH3COOH2+
(D) H2S dan S2–
(E) H2O dan OH–
Pembahasan Soal Kimia SBMPTN 2018 Nomor 34 Kode: 418, 460, 463
Ciri dari pasangan asam basa konjugasi yaitu kemiripan rumus kimia dengan selisih jumlah H sebanyak satu atom H.
H2S dan S2– bukan pasangan asam-basa konjugasi karena selisih jumlah atom H lebih dari 1.
Persiapan SBMPTN 2019 | Kunci Jawaban Soal Kimia SBMPTN 2018 Nomor 34 D.

2 Komentar